
去年5月,食品和药物管理局(FDA)发布了关于3D打印医疗设备的准则草案,当时天工社有对此进行过报导。昨日(12月7日),FDA对有关技术发布进一步指导。《FDA发布3D打印医疗设备的技术准则草案》FDA专员斯科特·戈特利布博士发表了一份声明,详细说明该机构一直在与3D打印医疗产品的新时代合作,并指出FDA已经审查了目前市场上的100多种3D打印设备,包括特定植入物和膝关节置换以及第一个3D打印药物。FDA发布的指导目的是为医疗设备制造商提供有关3D打印技术方面的建议,以及在3D打印医疗设备意见书方面提供明确的代理建议。

戈特利布解释说:“这包括我们对各种3D打印方法的思考,包括设备设计,功能和耐用性测试以及质量系统的要求。总的来说,这将有助于制造商通过为未来提供一个透明的流程,从而更有效地将其创新成果推向市场,并确保我们的监管方法能够适当地适应这种有前景的新技术所带来的独特机遇和挑战。”
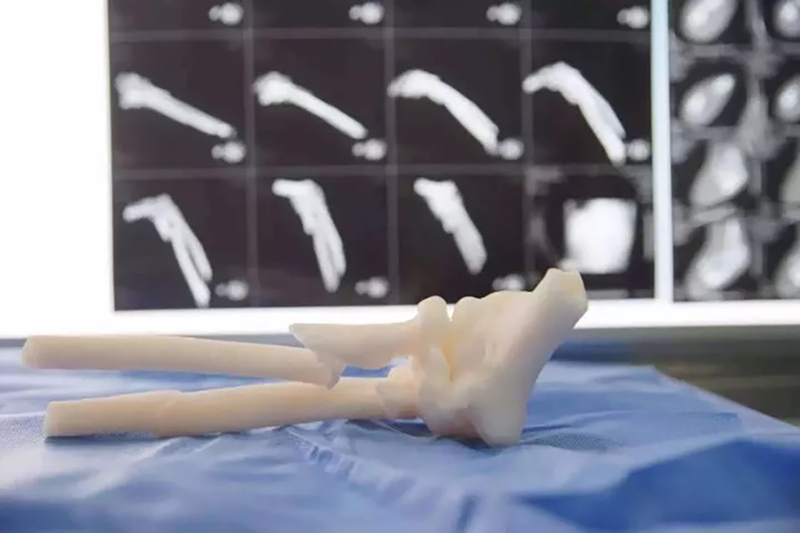
FDA正在建立一个监管框架,关于如何将其现有设备制造的管理条例规定应用到3D打印这些设备的体系和设施当中。根据戈特利布的声明,该机构是世界上第一个“综合技术框架”,将为制造商提供有关3D打印医疗产品的建议。FDA还计划审查与生物,细胞和组织产品生物打印有关的监管问题,以确定是否需要在最近发布的再生医学医疗产品监管框架之外提供额外的指导。戈特利布在声明中明确表示,这项新的技术指导仅仅是为了提供该机构对3D打印技术的想法,并指出FDA在3D打印方面提出的任何建议都很可能随着技术以意想不到的方式发展而演变。
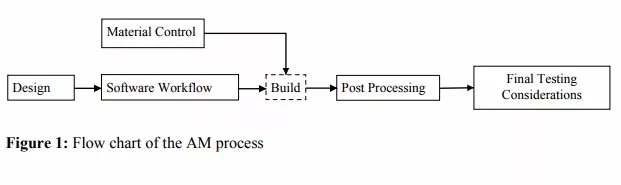
戈特利布总结说:“这些措施是我们努力范围的其中一部分,以确保我们的监管框架与我们被要求审查的新技术的独特属性相匹配。3D打印必然会改变医学的日常实践,患者将接受专门为他们定制的医疗产品的治疗。FDA肩负着重要使命,帮助动进这些努力,同时保护那些依靠医疗产品的患者的安全。”
 浙公网安备 33010602006102号
DESIGN BY :
WEETOP
浙公网安备 33010602006102号
DESIGN BY :
WEETOP